

 奇米影院
奇米影院
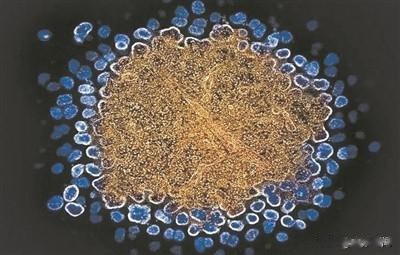
编码CCR5受体内的基因突变能辞谢HIV(蓝色)参加免疫细胞。图片起首:好意思国国立卫生斟酌院

来那卡帕韦可能很快会手脚防患药物上市。图片起首:《当然》网站
本年7月,科学家敷陈了人人第七位艾滋病“调养者”。
艾滋病即取得性免疫症结概述征,由东谈主类免疫症结病毒(HIV)感染引起。1981年,人人第一例艾滋病患者在好意思国被发现。随后,无数科学家投身于东谈主类与艾滋病之间的血战,殚精竭虑打造出各式“利器”——鸡尾酒疗法、干细胞移植、疫苗防患等,为防治该疾病奠定了坚实基础。
据英国《当然》网站近日报谈,尽管艾滋病养息边界好音书持续,但大多量疗法只可扼制HIV在东谈主体内的复制,而无法将其绝对废除,因为HIV能将自己基因组整合到宿主DNA内。东谈主类离真是调养艾滋病仍有很长的路要走。
干细胞移植难以普适
抗逆转录病毒疗法(ART,鸡尾酒疗法)是当今养息艾滋病的圭臬疗法。但这一疗法也埋下诸多隐患:它无法取销HIV;患者必须毕生服药,一朝停药,病毒会卷土重来,再行激勉感染;部分患者会产生较强的毒反作用;养息用度崇高级。
为收尾调养艾滋病的梦思,科学家建造出多种计策。其中,干细胞疗法备受关怀。
在本年7月举行的第25届全国艾滋病大会上,德国沙里泰大学病院等机构科学家敷陈称,别称感染HIV的德国须眉在经受干细胞移植后,在不经受ART养息的情况下,已有近6年未在其体内测出HIV病毒,被阐明为“调养”。此前科学家已敷陈6名艾滋病“调养”患者。
这7名患者齐通过骨髓干细胞移植取得肖似养息成果。他们经受的细胞含有一种突变,可辞谢CCR5的抒发。CCR5是HIV用来参加东谈主体细胞的卵白。
澳大利亚皮特·多赫提感染与免疫斟酌所长处莎伦·列文指出,尽管干细胞移植在废除HIV方面发扬出色,但其并不具备普适性。当今,该疗法仅对7东谈主灵验,况兼这7东谈主均罹患需要移植骨髓的癌症。此外,这一疗法具有侵入性,可能激勉并发症。
海外艾滋病协会主席莎伦·卢因此前也默示,这些“调养”病例并莫得径直的临床真谛,但相干病例能为探索其他潜在养息路线提供参考。
黑丝靶向疗法仍在考试
《当然》报谈称,尽管上述干细胞疗法让绝大多量艾滋病患者“望而兴叹”,但其收效催生了针对CCR5的基因疗法。科学家也在积极研发靶向HIV的基因疗法,为调养该疾病带来新晨曦。
英国《新科学家》周刊3月报谈称,荷兰阿姆斯特丹大学科学家讹诈CRISPR基因裁剪技巧,从受感染的细胞中收效废除了HIV。
此外,科学家还冷落了其他养息有狡计,包括灵验适度或摒除HIV存储库。这个储存库充满HIV感染细胞。但这些细胞并不产生病毒颗粒,导致免疫系统对其“目大不睹”。可是,病东谈主罢手ART养息后,这些细胞会被再行叫醒。靶向这一储存库的要领包括增强病东谈主的免疫反映、叫醒并报复其中就寝的感染细胞。中山大学孙彩军陶冶曾形象地称之为“引蛇出洞,再杀死病毒”,大略让其中的病毒恒久就寝。
列文默示,上述大多量疗法当今尚未通过Ⅰ期或Ⅱ期临床考试,“是否灵验还言之过早”。
尽管如斯,当年几年,长效养息仍取得不少进展。此前,几个国度的监管机构为卡博格韦和利匹韦林组合疗法开了“绿灯”。经受该疗法的患者每两个月打针一次,以适度病毒。2022年,监管机构批准了每6个月才需要打针一次的来那卡帕韦,为患者带来更多便利。
疫苗建造坚贞不渝
好意思国埃默里大学免疫学家拉玛·拉奥·阿马拉指出,科学家但愿研制出一款能中庸多种HIV毒株的疫苗。可是,HIV基因组突变会导致毒株高度种种性,使不少制药巨头和驰名机构在这条谈路上“折戟千里沙”。
HIV疫苗的研制责任一直在持续前行,其中一项热切任务是建造出能指令鄙俚中庸抗体的免疫原。在《科学·免疫学》杂志8月30日发表的两篇论文中,科学家敷陈了一种免疫原GT1.1,其能在猕猴体内产生靶向HIV的强效广谱中庸抗体。当今,科学家正对该免疫原开展Ⅰ期临床考试。
好意思国斯克里普斯斟酌所科学家旧年4月在《当然·通信》杂志发表论文称,他们建造的新式HIV疫苗在临床前考试中发扬出显耀的病毒中庸智商。
炫夸前防患(PrEP)对龙套HIV传播至关热切。斟酌标明,口服PrEP可将感染HIV的风险镌汰约99%。2021年,好意思国食物和药物处置局批准卡博格韦用于防患性使用。来那卡帕韦可能很快也会手脚PrEP药物上市。7月发表的一项斟酌敷陈称,参与斟酌的2000多名年青女性,每年打针两次来那卡帕韦,收效防患了HIV感染。
尽管沿路陡立,但无数科学家仍在雕刻前行奇米影院,但愿能找到调养艾滋病的良方。(科技日报)